Neutralización y Diluciones
¿Qué es la neutralización?
Reacción de neutralización:
Es una reacción de doble
desplazamiento o intercambio entre un ácido y una base, generalmente en las
reacciones acuosas ácido–base se forma sal y agua.
Ácido (ac) + Base (ac) ---------->
Sal (ac) + Agua (l)
También es una reacción de
sintesís o composición entre un óxido ácido (óxido no metálico) con un óxido
básico (oxido metálico), se forma sal.
Óxido ácido (g) + Óxido básico
(s) ----------> Sal (s)
Ejemplos:
Ácido clorhídrico + Hidróxido de
sodio ----------> Cloruro de sodio + Agua
HCl (ac) + NaOH (ac)
----------> NaCl (ac) + H2O (l)
Ácido sulfúrico + Hidróxido de
aluminio ----------> Sulfato de aluminio + Agua
3 H2SO4 (ac) + 2 Al(OH)3 (ac) ---------->
Al2(SO4)3 (ac) + 6 H2O (l)
Óxido de magnesio + Anhídrido
sulfúrico ----------> Sulfato de magnesio
MgO (s) + SO3 (g) ----------> MgSO4 (s)
Si al cocinar un caldo te sale
muy salado y lo quieres con sabor más suave ¿qué puedes hacer?. Y si el color
de una pintura es demasiado intenso y quieres rebajarlo ¿qué haces?. Muy
sencillo: añades agua, con lo que obtienes una disolución más diluida, con
menor sabor o color.
Las disoluciones concentradas que
no se utilizan normalmente, se guardan en el almacén del laboratorio. Con
frecuencia estas disoluciones se diluyen antes de utilizarlas.
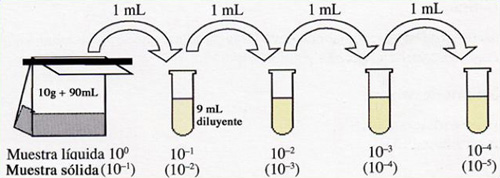
La dilución es el procedimiento
que se sigue para preparar una disolución menos concentrada a partir de una más
concentrada. El procedimiento es muy simple: solamente hay que tomar disolución
inicial y añadirle agua. El volumen de disolución a tomar y la cantidad de agua
a añadir dependen del volumen de disolución diluida que se quiera preparar, así
como de su concentración.
NOTA: ac: acuosa, l: líquido, g:
gaseoso y s: solido ,indica el etado en que se encuentra los elementos o
compuestos en las reacciones químicas.

No hay comentarios:
Publicar un comentario